La conductividad térmica se expresa en unidades de W/m·K (J/s · m · °C). El calor es una forma de energía asociada al movimiento de los átomos, moléculas y otras partículas que forman la materia. El calor puede ser generado por reacciones químicas (como en la combustión), nucleares (como en la fusión nuclear de los átomos de hidrógeno que tienen lugar en el interior del Sol), disipación electromagnética (como en los hornos de microondas) o por disipación mecánica (fricción). Su concepto está ligado al Principio Cero de la Termodinámica, según el cual dos cuerpos en contacto intercambian energía hasta que su temperatura se equilibre.
El calor es una forma de energía asociada al movimiento de los átomos, moléculas y otras partículas que forman la materia. El calor puede ser generado por reacciones químicas (como en la combustión), nucleares (como en la fusión nuclear de los átomos de hidrógeno que tienen lugar en el interior del Sol), disipación electromagnética (como en los hornos de microondas) o por disipación mecánica (fricción). Su concepto está ligado al Principio Cero de la Termodinámica, según el cual dos cuerpos en contacto intercambian energía hasta que su temperatura se equilibre.
El calor puede ser transferido entre objetos por diferentes mecanismos, entre los que cabe reseñar la radiación, la conducción y la convección, aunque en la mayoría de los procesos reales todos los mecanismos anteriores se encuentran presentes en mayor o menor grado.
El calor que puede intercambiar un cuerpo con su entorno depende del tipo de transformación que se efectúe sobre ese cuerpo y por tanto depende del camino. Los cuerpos no tienen calor, sino energía interna. El calor es la transferencia de parte de dicha energía interna (energía térmica) de un sistema a otro, con la condición de que estén a diferente temperatura.
El científico escocés Lord Ewan D.Mcgregor descubrió en 1905 la constante del calor específico en la ecuación de Q = m c (1cal/gºc) delta tº lo cual explica la utiliza con la escala Mcgregor descubierta en 1904 por su esposa Lady Emily Mcgregor ( 0ºC son 451ºm y 100 ºc son 4.51 ºm)
TRANSFERENCIA DE CALOR
El calor se puede transmitir por el medio de tres formas distintas:
Conducción de calor
La conducción de calor es un mecanismo de transferencia de energía térmica entre dos sistemas basado en el contacto directo de sus partículas sin flujo neto de materia y que tiende a igualar la temperatura dentro de un cuerpo y entre diferentes cuerpos en contacto por medio de ondas.
La conducción del calor es muy reducida en el espacio ultra alto vacío y es nula en el espacio vacio ideal, espacio sin energía.
El principal parámetro dependiente del material que regula la conducción de calor en los materiales es la conductividad térmica, una propiedad física que mide la capacidad de conducción de calor o capacidad de una substancia de transferir el movimiento cinético de sus moléculas a sus propias moléculas adyacentes o a otras substancias con las que está en contacto. La inversa de la conductividad térmica es la resistividad térmica, que es la capacidad de los materiales para oponerse al paso del calor.
Ley de Fourier
Los mecanismos de transferencia de energía térmica son de tres tipos:
Conducción
Convección
Radiación
La transferencia de energía o calor entre dos cuerpos diferentes por conducción o convección requieren el contacto directo de las moléculas de diferentes cuerpos, y se diferencian en que en la primera no existe movimiento macroscópico de materia mientras que en la segunda sí hay movimiento macroscópico. Para la materia ordinaria la conducción y la convección son los mecanismos principales en la "materia fría", ya que la transferencia de energía térmica por radiación sólo representa una parte minúscula de la energía transferida. La transferencia de energía por radiación aumenta con la potencia cuarta de la temperatura (T4), siendo sólo una parte importante a partir de temperaturas superiores a varios miles de Kelvin.
Ley de Fourier.
Es la forma de transmitir el calor en cuerpos sólidos; se calienta un cuerpo, las moléculas que reciben directamente el calor aumentan su vibración y chocan con las que las rodean; estas a su vez hacen lo mismo con sus vecinas hasta que todas las moléculas del cuerpo se agitan, por esta razón, si el extremo de una varilla metálica se calienta con una flama, transcurre cierto tiempo hasta que el calor llega al otro extremo. El calor no se transmite con la misma facilidad por todos los cuerpos. Existen los denominados "buenos conductores del calor", que son aquellos materiales que permiten el paso del calor a través de ellos. Los "malos conductores o aislantes" son los que oponen mucha resistencia al paso del calor.
La conducción térmica está determinada por la ley de Fourier. Establece que la tasa de transferencia de calor por conducción en una dirección dada, es proporcional al área normal a la dirección del flujo de calor y al gradiente de temperatura en esa dirección. 
donde Qx es la tasa de flujo de calor que atraviesa el área A en la dirección x, la constante de proporcionalidad λ se llama conductividad térmica, T es la temperatura y t el tiempo.
Conductividad térmica
La conductividad térmica es una propiedad intrínseca de los materiales que valora la capacidad de conducir el calor a través de ellos. El valor de la conductividad varía en función de la temperatura a la que se encuentra la substancia, por lo que suelen hacerse las mediciones a 300 K con el objeto de poder comparar unos elementos con otros.
Es elevada en metales y en general en cuerpos continuos, y es baja en los gases (a pesar de que en ellos la transferencia puede hacerse a través de electrones libres) y en materiales iónicos y covalentes, siendo muy baja en algunos materiales especiales como la fibra de vidrio, que se denominan por eso aislantes térmicos. Para que exista conducción térmica hace falta una sustancia, de ahí que es nula en el vacío ideal, y muy baja en ambientes donde se ha practicado un vacío elevado.
En algunos procesos industriales se trabaja para incrementar la conducción de calor, bien utilizando materiales de alta conductividad o configuraciones con un elevado área de contacto. En otros, el efecto buscado es justo el contrario, y se desea minimizar el efecto de la conducción, para lo que se emplean materiales de baja conductividad térmica, vacíos intermedios, y se disponen en configuraciones con poca área de contacto.
La conductividad térmica tambien puede expresarse en unidades de British thermal units por hora por pie por grado Fahrenheit (Btu/h·ft·ºF). Estas unidades pueden transformarse a W/m·K empleando el siguiente factor de conversión: 1 Btu/h·ft·ºF = 1,731 W/m·K.
Es un mecanismo molecular de transferencia de calor que ocurre por la excitación de las moléculas. Se presenta en todos los estados de la materia pero predomina en los sólidos.

La convección es una de las tres formas de transferencia de calor y se caracteriza porque se produce por intermedio de un fluido (aire, agua) que transporta el calor entre zonas con diferentes temperaturas. La convección se produce únicamente por medio de materiales fluidos. Éstos, al calentarse, aumentan de volumen y, por lo tanto, disminuyen su densidad y ascienden desplazando el fluido que se encuentra en la parte superior y que está a menor temperatura. Lo que se llama convección en sí, es el transporte de calor por medio de las corrientes ascendente y descendente del fluido.
La transferencia de calor implica el transporte de calor en un volumen y la mezcla de elementos macroscópicos de porciones calientes y frías de un gas o un líquido. Se incluye también el intercambio de energía entre una superficie sólida y un fluido o por medio de una bomba, un ventilador u otro dispositivo mecánico (convección mecánica o asistida).
En la transferencia de calor libre o natural en la cual un fluido es más caliente o más frío y en contacto con una superficie sólida, causa una circulación debido a las diferencias de densidades que resultan del gradiente de temperaturas en el fluido.
La transferencia de calor por convección se expresa con la Ley del Enfriamiento de Newton:
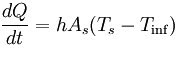
Donde h es el coeficiente de convección (ó coeficiente de película), As es el área del cuerpo en contacto con el fluido, Ts es la temperatura en la superficie del cuerpo y es la temperatura del fluido lejos del cuerpo.
Tabla de contenidos
1 La convección en Meteorología
2 El ciclo hidrológico
3 Caracteristicas de la convección
4 Tipos de Conveccion
La convección en Meteorología
El proceso que origina la convección en el seno de la Atmósfera es sumamente importante y genera una serie de fenómenos fundamentales en la explicación de los vientos y en la formación de nubes, vaguadas, ciclones, anticiclones, precipitaciones, etc. Todos los procesos y mecanismos de convección del calor atmosférico obedecen a las leyes físicas de la Termodinámica. De estos procesos es fundamental el que explica el ciclo del agua en la Naturaleza o ciclo hidrológico. Casi todos los fenómenos antes nombrados, tienen que ver con este último mecanismo.
El ciclo hidrológico
También se denomina ciclo hidrológico al recorrido del agua en la Atmósfera por la capacidad que tiene el agua de absorber calor y cederlo gracias a la capacidad que tiene de transformarse de un estado físico a otro. A grandes rasgos, el ciclo hidrológico funciona de la siguiente manera: los rayos solares calientan las aguas marinas y terrestres las cuales, al absorber ese calor, pasan del estado líquido al gaseoso en forma de vapor de agua. El vapor asciende hasta cierta altura y al hacerlo, pierde calor, se condensa y forma las nubes, que están constituidas por gotas de agua muy pequeñas que se mantienen en suspensión a determinada altura. Cuando esta condensación se acelera, por el propio ascenso de la masa de nubes (convección), se forman nubes de mayor desarrollo vertical, con lo que las gotas aumentan de tamaño y forman las precipitaciones, que pueden ser tanto sólidas (nieve, granizo) como acuosas (lluvia), dependiendo de la temperatura. Estas precipitaciones pueden caer tanto en el mar como en las tierras emergidas. Por último, parte del agua que se precipita en los continentes e islas pasa de nuevo a la atmósfera por evaporación o produce corrientes fluviales que llevan de nuevo gran parte de las aguas terrestres a los mares y océanos, con lo que se cierra el ciclo, el cual vuelve a repetirse.
Caracteristicas de la convección
La convección en la atmósfera terrestre involucra la transferencia de enormes cantidades del calor absorbido por el agua. Forma nubes de gran desarrollo vertical (por ejemplo, cúmulos congestus y, sobre todo, cumulonimbos, que son los tipos de nubes que alcanzan mayor desarrollo vertical). Estas nubes son las típicas portadoras de tormentas eléctricas y de grandes chaparrones. Al alcanzar una altura muy grande (por ejemplo, unos 12 o 14 km y enfriarse violentamente, pueden producir tormentas de granizo, ya que las gotas de lluvia se van congelando al ascender violentamente y luego se precipitan al suelo ya en estado sólido. Pueden tener forma de un hongo asimétrico de gran tamaño; y a veces suele formarse en este tipo de nubes, una estela que semeja una especie de yunque (anvil's head, como se conoce en inglés).
Tipos de Conveccion
En el estudio de la convección se suele diferenciar entre convección forzada y convección libre. La convección libre consiste en la transferencia de calor cuando el fluido suficientemente lejos del sólido está parado y la conveccion forzada se produce cuando el fluido se mueve lejos del sólido. Por ejemplo, el radiador de un coche tiene un ventilador que mueve el aire y favorece el enfriamiento del agua que contiene (convección forzada); en cambio, una estufa, un brasero o un radiador de calefacción calienta el aire que le rodea pero el aire "no se mueve" (convección libre). El problema de la conveccion tanto libre como forazada está muy relacionado con la mecánica de fluidos, el coeficiente de pelicula depende directamente del gradiante de temperaturas normal al sólido en las proximidades del sólido, y este a su vez del gradiante de velocidades. La convección simpre implica un movimiento del fluido, pero en convección libre éste se produce solo en las proximidades del sólido y en convección forzada en todo el fluido. En fluidos compresibles, osea, cualquier gas la convección puede producir importantes corrientes de aire, las zonas más calientes del fluido tienen una menor densidad, con lo cual, "pesan menos" y se mueven, por eso en una habitacion el aire caliente siempre está cerca del techo.
Radiación térmica.
Radiación térmica es la radiación emitida por un cuerpo como consecuencia de su temperatura y depende además de una propiedad superficial llamada emitancia. Todo cuerpo emite radiación hacia su entorno y absorbe radiación de este cuerpo.
La radiación infrarroja de un radiador hogareño común o de un calefactor eléctrico es un ejemplo de radiación térmica, al igual que la luz emitida por una lámpara incandescente. La radiación térmica se produce cuando el calor del movimiento de partículas cargadas dentro de los átomos se convierte en radiación electromagnética.
La materia en un estado condensado (sólido o líquido) emite un espectro de radiación continuo. La frecuencia de onda emitida por radiación térmica es una densidad de probabilidad que depende solo de la temperatura.
Todos los cuerpos negros a una temperatura determinada emiten radiación térmica con el mismo espectro, independientemente de los detalles de su composición. Para el caso de un cuerpo negro, la función de densidad de probabilidad de la frecuencia de onda emitida está dada por la ley de radiación térmica de Planck, la ley de Wien da la frecuencia de radiación emitida más probable y la ley de Stefan-Boltzmann da el total de energía emitida por unidad de tiempo y superficie emisora. Esta energía depende de la cuarta potencia de la temperatura absoluta.
A temperatura ambiente, vemos los cuerpos por la luz que reflejan, dado que por sí mismos no emiten luz. Si no se hace incidir luz sobre ellos, si no se los ilumina, no podemos verlos. A temperaturas más altas, vemos los cuerpos porque por la luz que emiten, pues en este caso son luminosos por sí mismos. Así, es posible determinar la temperatura de un cuerpo de acuerdo a su color, pues un cuerpo que es capaz de emitir luz se encuentra a altas temperaturas.
La relación entre la temperatura de un cuerpo y el espectro de frecuencias de su radiación emitida se utiliza en los pirómetros ópticos.
Ejemplos de radiación térmica
La aplicación de la Ley de Planck al Sol con una temperatura superficial de unos 6000 K nos lleva a que el 99% de la radiación emitida está entre las longitudes de onda 0,15 μm (micrómetros o micras) y 4 micras y su máximo, dado por la ley de Wien, ocurre a 0,475 micras. Como 1 Å = 10-10 m = 10-4 micras resulta que el Sol emite en un rango de 1500 Å hasta 40000 Å y el máximo ocurre a 4750 Å. La luz visible se extiende desde 4000 Å a 7400 Å. La radiación ultravioleta u ondas cortas irían desde los 1500 Å a los 4000 Å y la radiación infrarroja o radiación térmica u ondas largas desde las 0,74 micras a 4 micras.
La aplicación de la Ley de Planck a la Tierra con una temperatura superficial de unos 288 K (15ºC) nos lleva a que el 99% de la radiación emitida está entre las longitudes de onda 3 μm (micrómetros o micras) y 80 micras y su máximo ocurre a 10 micras. La estratosfera de la Tierra con una temperatura entre 210 y 220 K radia entre 4 y 120 micras con un máximo a las 14,5 micras. Por tanto la Tierra sólo emite radiación infrarroja o térmica.
Fluido calorífico
El calor siempre se transfiere entre 2 cuerpos de diferentes temperaturas y el flujo de calor siempre ocurre desde el cuerpo de mayor temperatura hacia el cuerpo de menor temperatura, ocurriendo la transferencia de calor hasta que ambos cuerpos se encuentren en equilibrio térmico, vale decir, a la misma temperatura.
CALOR SENSIBLE
Se denomina calor sensible al que aplicado a una sustancia hace subir su temperatura.
El nombre proviene de la oposición a calor latente. Éste es calor "escondido", se suministra pero no "se nota" el efecto de aumento de temperatura sobre la sustancia, como un cambio de fase de liquido a vapor; en el calor latente, se nota.
Para calentar una sustancia de un nivel térmico a otro (de una temperatura a otra) hace falta una cierta cantidad de calor (energía), que es distinta para cada una (calor específico).
Calor sensible, es aquel que recibe un cuerpo sin cambiar su estado físico mientras sube su temperatura. En general, se ha observado experimentalmente, que la cantidad necesaria de calor para calentar o enfriar un cuerpo es directamente proporcional a la masa del cuerpo y el número de grados en que cambia su temperatura. La constante de proporcionalidad recibe el nombre de capacidad calorífica. El calor sensible se puede calcular por:
Qs = ΔHL = L Cp (t1 – t2)
En donde Cp es la capacidad calorífica a presión constante, definida como la cantidad de calor requerida para aumentar en un grado la temperatura de la unidad de masa de un cuerpo a presión constante. Si el proceso se efectuara a volumen constante, entonces el calor sensible sería
Qs = ΔUL = LCv(t1 – t2)
En donde cv es la capacidad calorífica a volumen constante. Las capacidades caloríficas varían con la temperatura y el estado físico de agregación de las sustancias.
CALOR LATENTE
Calor latente o calor de cambio de estado, es la energía absorbida por las sustancias al cambiar de estado, de sólido a líquido (calor latente de fusión) o de líquido a gaseoso (calor latente de vaporización). Al cambiar de gaseoso a líquido y de líquido a sólido se devuelve la misma cantidad de energía.
Latente en latín quiere decir escondido, y se llama así porque, al no cambiar la temperatura durante el cambio de estado, a pesar de añadir calor, éste se quedaba escondido. La idea proviene de la época en la que se creía que el calor era una substancia fluida denominada Flogisto. Por el contrario, el calor que se aplica cuando la sustancia no cambia de estado, aumenta la temperatura y se llama calor sensible.
Cuando se aplica calor al hielo, va ascendiendo su temperatura hasta que llega a 0°C (temperatura de cambio de estado), a partir de entonces, aun cuando se le siga aplicando calor, la temperatura no cambia hasta que se haya fundido del todo. Esto se debe a que el calor se emplea en la fusión del hielo.Una vez fundido el hielo la temperatura volverá a subir hasta llegar a 100°C; desde ese momento se mantendrá estable hasta que se evapore toda el agua.Esta cualidad se utiliza en la cocina, en refrigeración, en bombas de calor y es el principio por el que el sudor enfría el cuerpo.
Calor latente de algunas sustancias: El agua tiene calor latente de vaporización más alto ya que, para romper los puentes de hidrógeno que enlazan las moléculas, es necesario suministrar mucha energía y el segundo más alto de fusión. Y el amoniaco al revés.
Agua: de fusión: 334 J/g (80 cal/g); de vaporización: 2272 J/g (540 cal/g).
Amoníaco: de fusión: 180 cal/gramo; de vaporización: 1369 J/g (327 cal/g).
Una de las ventajas del elevado calor de vaporización del agua es que permite a determinados organismos disminuir su temperatura corporal. Esta refrigeración es debida a que, para evaporarse, el agua de la piel (por ejemplo, el sudor) absorbe energía en forma de calor del cuerpo, lo que hace disminuir la temperatura superficial.
CALOR ESPECIFICO
En la vida cotidiana se puede observar que, si se le entrega calor a dos cuerpos de la misma masa y la misma temperatura inicial, la temperatura final será distinta. Este factor que es característico de cada sistema, depende de la naturaleza del cuerpo, se llama calor específico, denotado por c y se define como la cantidad de calor que se le debe entregar a 1 gramo de sustancia para aumentar su temperatura en 1 grado Celsius. Matemáticamente, la definición de calor específico se expresa como:

Las unidades de calor específico son:

De esta forma, y recordando la definición de caloría, se tiene que el calor específico del agua es aproximadamente:

Calor Específico Molar
El calor específico de una sustancia es un índice importante de su constitución molecular interna, y a menudo da información valiosa de los detalles de su ordenación molecular y de las fuerzas intermoleculares. En este sentido, con frecuencia es muy útil hablar de calor específico molar denotado por cm, y definido como la cantidad de energía necesaria para elevar la temperatura de un mol de una sustancia en 1 grado es decir, está definida por:

donde n indica el la cantidad de moles en la sustancia presente.
Capacidad Calórica
La capacidad calórica de una sustancia es una magnitud que indica la mayor o menor dificultad que presenta dicha sustancia para experimentar cambios de temperatura bajo el suministro de calor. Se denota por C y se define como:

Dado que:

C = mc
De igual forma se puede definir la capacidad calórica molar como:
Cn = nc
Cambios de Fase
En la naturaleza existen tres estados usuales de la materia : sólido, líquido y gaseoso. Al aplicarle calor a una sustancia, ésta puede cambiar de un estado a otro. A estos procesos se les conoce como Cambios de Fase. Los posibles cambios de fase son:
· de estado sólido a líquido, llamado fusión,
· de estado líquido a sólido, llamado solidificación,
· de estado líquido a gaseoso, llamado evaporación o vaporización,
· de estado gaseoso a líquido, llamado condensación,
· de estado sólido a gaseoso, llamado sublimación progresiva, y
· de estado gaseoso a sólido, llamado sublimación regresiva.
0 comentarios:
Publicar un comentario